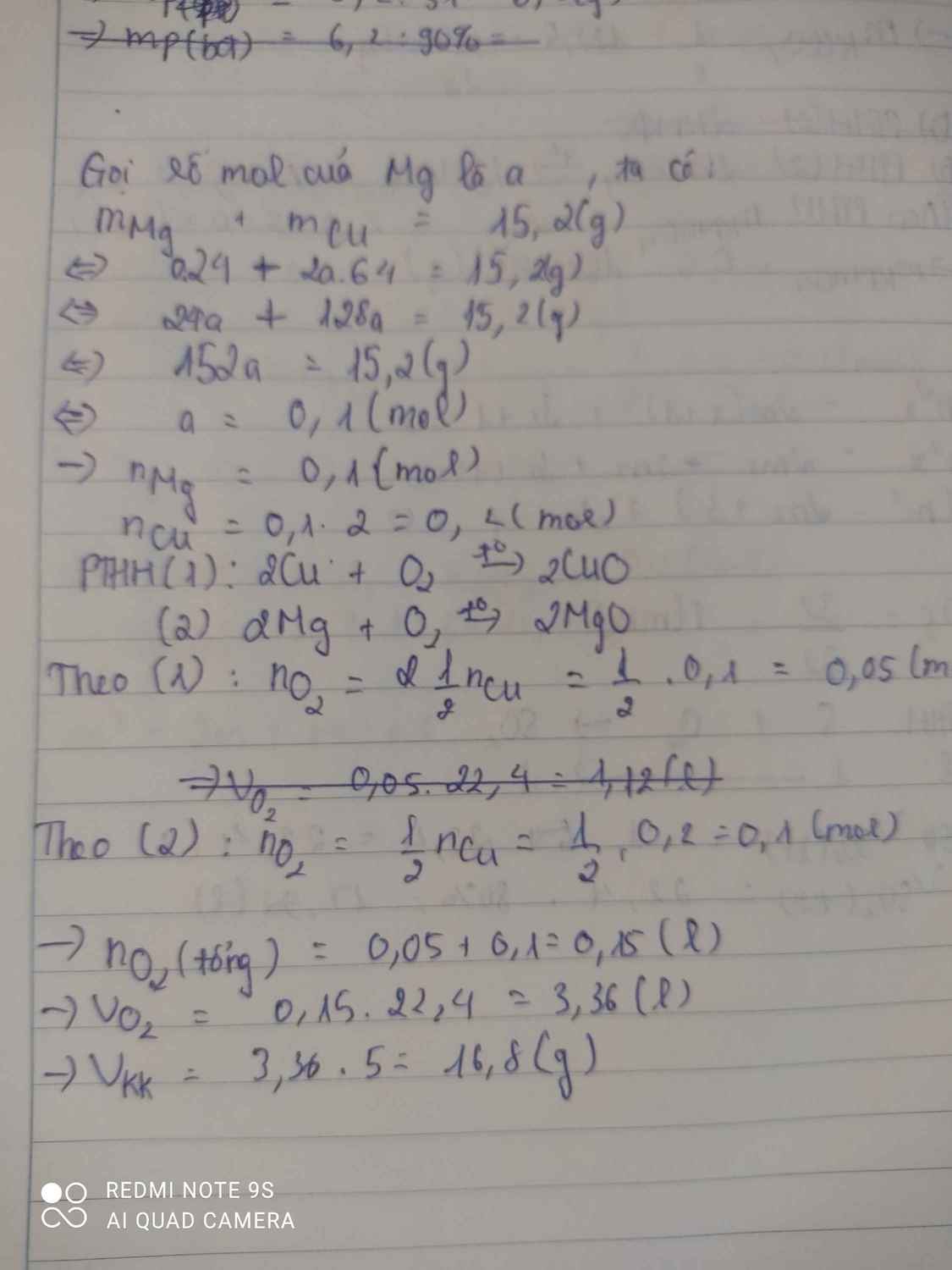Những câu hỏi liên quan
1) đốt cháy M gam hỗn hợp AL và Củ trong 3,92lít oxi,sau pứ thu đc 21,1gam oxit.tính % khối lượng mỗi chất trong hỗn hợp đầu.
Câu 2) đốt cháy hoàn toàn hỗn hợp CH4 và C3H8 trong khí oxi, sau pứ thu dc 12,6gam nước. Tính %thể tích và % hỗn hợp đâù
Mn giúp e vs e cần gấp ạ
Xem chi tiết
Câu 1:
Đặt \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Cu}=b\left(mol\right)\end{matrix}\right.\)\(\Rightarrow\left\{{}\begin{matrix}n_{CuO}=n_{Cu}=b\left(mol\right)\\n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=\dfrac{1}{2}a\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow102\cdot\dfrac{1}{2}a+80b=21,1\) (1)
Ta có: \(n_{O_2}=\dfrac{3,92}{22,4}=0,175\left(mol\right)\)
Bảo toàn electron: \(3a+2b=0,7\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,1\cdot27=2,7\left(g\right)\\m_{Cu}=0,2\cdot64=12,8\left(g\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{2,7}{2,7+12,8}\cdot100\%\approx17,42\%\\\%m_{Cu}=82,58\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 5,6 lit hỗn hợp khí X gồm (CH4 và C3H8) ở đktc, sau phản ứng thu được 10,8g H20. Tính % về thể tích của mỗi khí trong hỗn hợp X.
Giải giúp mình với ạ.
Gọi số mol CH4, C3H8 là a, b (mol)
=> \(a+b=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
a------------------------>2a
C3H8 + 5O2 --to--> 3CO2 + 4H2O
b---------------------------->4b
=> \(n_{H_2O}=2a+4b=\dfrac{10,8}{18}=0,6\left(mol\right)\)
=> a = 0,2; b = 0,05
=> \(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,2}{0,25}.100\%=80\%\\\%V_{C_3H_8}=\dfrac{0,05}{0,25}.100\%=20\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Câu 4: Đốt cháy một hỗn hợp gồm CH4 và C2H2 có thể tích là 33,6 lít (đktc) thu được 56 lít khí CO2 (đktc).a. Xác định thành phần % về thể tích các khí trong hỗn hợp?b. Tính khối lượng của oxi cần để đốt cháy hoàn toàn hỗn hợp khí trên?
Đọc tiếp
Câu 4: Đốt cháy một hỗn hợp gồm CH4 và C2H2 có thể tích là 33,6 lít (đktc) thu được 56 lít khí CO2 (đktc).
a. Xác định thành phần % về thể tích các khí trong hỗn hợp?
b. Tính khối lượng của oxi cần để đốt cháy hoàn toàn hỗn hợp khí trên?
a, \(CH_4+2O_2\underrightarrow{t^o}CO_2+H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Ta có: \(n_{CH_4}+n_{C_2H_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\left(1\right)\)
Theo PT: \(n_{CO_2}=n_{CH_4}+2n_{C_2H_2}=\dfrac{56}{22,4}=2,5\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,5\left(mol\right)\\n_{C_2H_2}=1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,5.22,4}{33,6}.100\%\approx33,33\%\\\%V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
b, Theo PT: \(n_{O_2}=2n_{CH_4}+\dfrac{5}{2}n_{C_2H_2}=3,5\left(mol\right)\Rightarrow m_{O_2}=3,5.32=112\left(g\right)\)
Đúng 3
Bình luận (1)
đốt cháy hoàn toàn 5,6 g hỗn hợp a gồm s và c (trong a, số mol của s gấp đôi số mol của c) trong không khí, sau phản ứng thu được hỗn hợp khí b. các thể tích khí đo ở đktc a) viết PTHH 2)thể tchs không khí tối thiểu cần đốt để đốt cháy hỗn hợp A, biết oxi chiếm 20% thể tích không c)tỉ khối b và ch4 khí
Đốt cháy hoàn toàn 15,2g hỗn hợp Cu và Mg trong không khí . Tính thể tích oxi và thể tích không khí ở đktc cần sử dụng , biết tong hỗn hợp số mol Cu gấp đôi số mol Mg
Giúp emm với ạ
PTHH: 2Cu + O2 ---to→ 2CuO
Mol: x 0,5x
PTHH: 2Mg + O2 ---to→ 2MgO
Mol: 0,5x 0,25x (do số mol của Cu gấp đôi Mg)
Ta có: \(64x+24.0,25x=15,2\Leftrightarrow x=\dfrac{38}{175}\left(mol\right)\)
\(\Rightarrow n_{O_2}=0,5.\dfrac{38}{175}+0,25.\dfrac{38}{175}=\dfrac{57}{350}\left(mol\right)\)
\(\Rightarrow V_{O_2}=\dfrac{57}{350}.22,4=3,648\left(l\right)\)
\(\Rightarrow V_{kk}=3,648.5=18,24\left(l\right)\)
Đúng 1
Bình luận (1)
PTHH : \(2Cu+O_2\left(t^o\right)->2CuO\) (1)
\(2Mg+O_2\left(t^o\right)->2MgO\) (2)
Gọi x là số mol của Mg lak x (x ∈ Z+)
Theo đề ra : \(n_{Cu}=2n_{Mg}\)
Lại có : \(m_{Cu}+m_{Mg}=15,2\left(g\right)\)
-> \(n_{Cu}.M_{Cu}+n_{Mg}.M_{Mg}=15,2\)
-> \(2.n_{Mg}.M_{Cu}+n_{Mg}.M_{Mg}=15,2\)
-> \(2.n_{Mg}.64+n_{Mg}.24=15,2\)
-> \(n_{Mg}.\left(128+24\right)=15,2\)
-> \(n_{Mg}=0.1\left(mol\right)\)
Vậy \(n_{Cu}=0.2\left(mol\right)\)
Từ (1) => \(\dfrac{1}{2}n_{Cu}=n_{O_2}=0.1\left(mol\right)\)
=> \(V_{O_2\left(1\right)}=n.22,4=2,24\left(l\right)\)
Từ (2) => \(\dfrac{1}{2}n_{Mg}=n_{O_2}=0.05\left(mol\right)\)
=> \(V_{O_2\left(2\right)}=n.22,4=1,12\left(l\right)\)
=> \(V_{O_2\left(PƯ\right)}=V_{O_2\left(1\right)}+V_{O_2\left(2\right)}=1,12+2,24=3,36\left(l\right)\)
Đúng 2
Bình luận (1)
Đốt cháy hoàn toàn m gam hỗn hợp gồm C2H2, CH4,C2H6, C4H10. sau phản ứng thu được 8,96 lít khí CO2 và 10,8 gam H2O.
a. tính m?
b. tính v không khí cần dùng để đốt cháy hết hỗn hợp trên? Biết Oxi chiếm 20% thể tích không khí
help me !!!!![]()
a, Ta có: \(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\Rightarrow n_H=0,6.2=1,2\left(mol\right)\)
m = mC + mH = 0,4.12 + 1,2.1 = 6 (g)
b, Theo ĐLBT KL, có: m + mO2 = mCO2 + mH2O
⇒ mO2 = 22,4 (g) \(\Rightarrow n_{O_2}=\dfrac{22,4}{32}=0,7\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,7.22,4=15,68\left(g\right)\)
\(\Rightarrow V_{kk}=\dfrac{15,68}{20\%}=78,4\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 8gam hỗn hợp X gồm CH4 và C2H4 qua ddich Br2 dư, sau pứ xảy ra hoàn toàn còn lại 3,36l (dktc)
a, Tính thành phần phần trăm theo thể tích mỗi khí trong hỗn hợp X
b, nếu đem đốt cháy hoàn toàn 8 gam hỗn hợp trên rồi dẫn toàn bộ sản phẩm thu được qua dung dịch Ca(OH)2 dư .Tính khối lượng kết tủa thu được sau phản ứng
a) Khí còn lại là CH4
\(n_{CH_4} = \dfrac{3,36}{22,4} = 0,15(mol)\\ n_{C_2H_4} = \dfrac{8-0,15.16}{28} = 0,2(mol)\)
Vậy :
\(\%m_{CH_4} = \dfrac{0,15.16}{8}.100\% = 30\%\\ \%m_{C_2H_4} = 100\% - 30\% = 70\%\)
b)
\(CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_4 + 2O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O\\ CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\\ n_{CaCO_3} = n_{CO_2} = n_{CH_4} + 2n_{C_2H_4} =0,55(mol)\\ m_{CaCO_3} =0,55.100 = 55(gam) \)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 6,72 lít hỗn hợp khí X (đktc) gồm CH4 và C2H2 thu được 7,2 gam nước. Tính % thể tích mỗi khí trong hỗn hợp ?
Ta có: \(n_{hhk}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_2}=y\left(mol\right)\end{matrix}\right.\)
⇒ x + y = 0,3 (1)
Có: \(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
____x__________________2x (mol)
\(C_2H_2+\dfrac{5}{2}O_2\underrightarrow{t^o}2CO_2+H_2O\)
__y__________________y (mol)
⇒ 2x + y = 0,4 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
Ở cùng điều kiện nhiệt độ và áp suất, % thể tích cũng là % số mol.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,1}{0,3}.100\%\approx33,33\%\\\%V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
Bạn tham khảo nhé!
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 6,72 lít hỗn hợp khí X (đktc) gồm CH4 và C2H2 thu được 7,2 gam nước. Tính % thể tích mỗi khí trong hỗn hợp ?
Sửa:
Ta có: \(n_{hh_X}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
Gọi x, y lần lượt là số mol của CH4 và C2H2
PTHH: \(CH_4+2O_2\overset{t^o}{--->}CO_2+2H_2O\left(1\right)\)
\(C_2H_2+\dfrac{5}{2}O_2\overset{t^o}{--->}2CO_2+H_2O\left(2\right)\)
Theo PT(1): \(n_{H_2O}=2.n_{CH_4}=2x\left(mol\right)\)
Theo PT(2): \(n_{H_2O}=n_{C_2H_2}=y\left(mol\right)\)
\(\Rightarrow2x+y=0,4\) (*)
Theo đề, ta lại có: \(x+y=0,3\) (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}2x+y=0,4\\x+y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow\%_{V_{CH_4}}=\dfrac{0,1}{0,3}.100\%=33,3\%\)
\(\%_{V_{C_2H_2}}=100\%-33,3\%=66,7\%\)
Đúng 1
Bình luận (0)
Ta có: \(n_{hh_X}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
Gọi x, y lần lượt là số mol của CH4 và C2H2
PTHH:
\(C_2H_4+3O_2--->2CO_2\uparrow+2H_2O\) (1)
\(C_2H_2+\dfrac{5}{2}O_2--->2CO_2\uparrow+H_2O\) (2)
Theo PT(1): \(n_{H_2O}=2.n_{C_2H_4}=2x\left(mol\right)\)
Theo PT(2): \(n_{H_2O}=n_{C_2H_2}=y\left(mol\right)\)
\(\Rightarrow2x+y=0,4\) (*)
Theo đề, ta lại có: \(x+y=0,3\) (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}2x+y=0,4\\x+y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow\%_{V_{CH_4}}=\dfrac{0,1}{0,3}.100\%=33,3\%\)
\(\%_{V_{C_2H_2}}=100\%-33,3\%=66,7\%\)
Đúng 0
Bình luận (0)